性能验证@正确度
正确度和前面的精密度都会直接影响着患者的诊断与治疗。所以我们在新仪器启动前或仪器有重大变化的时候,做好性能验证,对临床就十分重要。
正确度代表的是系统误差,以偏倚表示。按照EP15-A2的要求,可以有两种方法来验证,包括比对试验和测量标准物质。
正确度验证举例
文档中包含很多理论的内容,为了使表达更加更直观易懂,我继续引用前面的例子来解释一下。
我们打靶,打了200发子弹,那么这200次就会产生一个范围,范围的大小(离散程度,用不精密度来表示cv/s),打靶产生的这个正态分布的中心和标准的靶心之间的偏差(偏倚),就是我们要测量的正确度。如果这个偏倚太大太多,就不满足正确度的要求了。换做我们日常工作,也就是说我们的结果与真实的结果的偏差。这里的正确度验证,就是在验证我们的结果与真实结果之间的偏差是否满足要求。
接下来,我们一起来看一下如何验证我们的仪器的正确度!
参考规范
和前面的精密度验证一样,在WST492和EP15A2中有详细的介绍.
这里有两种方法来验证
方法A:参考物质
所谓的参考物质就是具有指定值的一些物质,可以包括经过参考方法或决定方法测量过的新鲜冰冻血清。
从能力对比实验室中获取的参考物(罗氏诊断、CAP、卫生部提供的室间质评等)
厂家提供的经过正确度确认血清或质控物等。
总之就是具有已知的正确数值的物质。
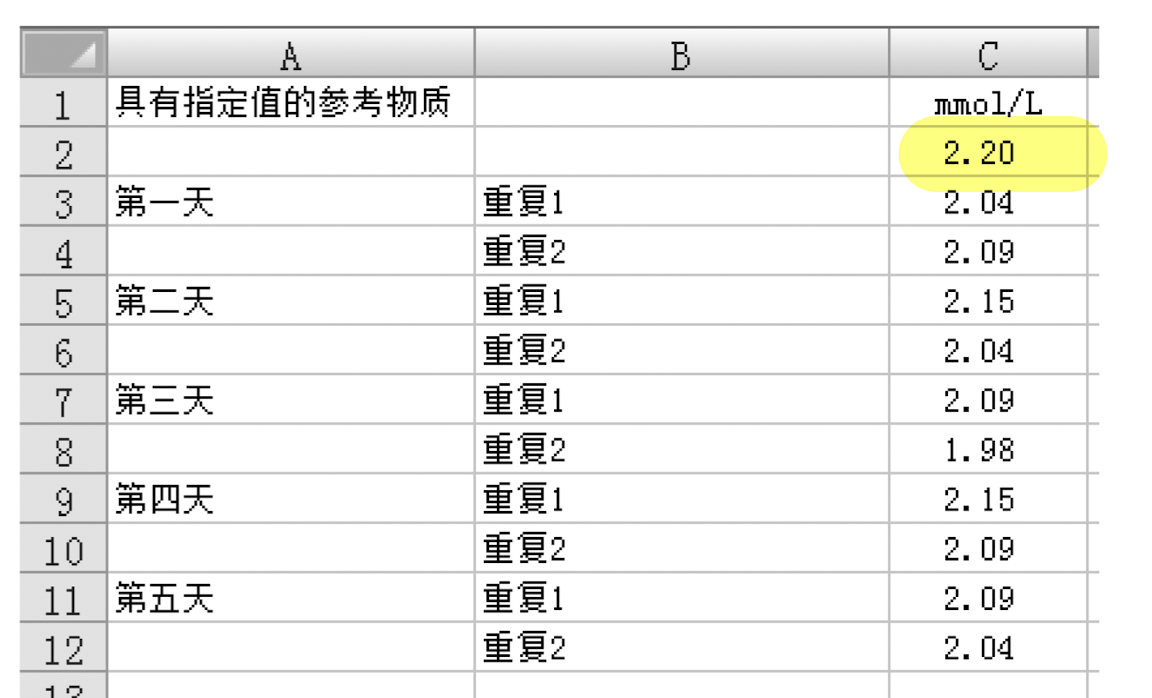
我们选择2个浓度的这样的参考物质,用3-5天,每个浓度每天做2次测定,然后计算均值、标准差,以及置信区间来验证。
下面是一个浓度的数据稿.
image-20211128173434711
假如这数据都已经收集完成了,我们接下来看看如何计算和验证。
方法A:计算与验证
计算过程我依旧简单说下(有兴趣的可以单独联系我),中间过程有:结果数量、均值、标准差、标准误、置信区间、合成不确定度、验证上下限。
具体的计算过程不算难,我这里就提一下关于置信区间和验证上下限的计算。
置信区间的意思是:通过你对参考物质的10次测量,会形成一个正态分布的数据集合,我们把这个集合的99%的区间用统计学的方式计算出一个范围,即置信区间。如果这个区间包含了参考物质的定值,那么就代表通过验证。
如果不包含,我们还可以把参考物质的不确定度也加入置信区间的计算,这样范围就会扩大一些,得到的验证上下限,如果这个验证的上下限包含了参考物质的定值,那么就代表通过验证。
如果不包含,那么就没有通过验证。
方法B:患者样本的方法比对
由于很多实验室,可能获取到参考物质比较困难。选择用患者样本做比对也是一种不错的方案,实际上这种验证方案,是两种方法之间的系统误差,如果选择的不是参考实验室的参考方法,也不能算作为真正的正确度验证,仅仅是两种方法之间的系统误差。
检测20分患者样本,浓度覆盖检测方法的可报告范围。在3-4天内完成。每天完成5-7份样本。
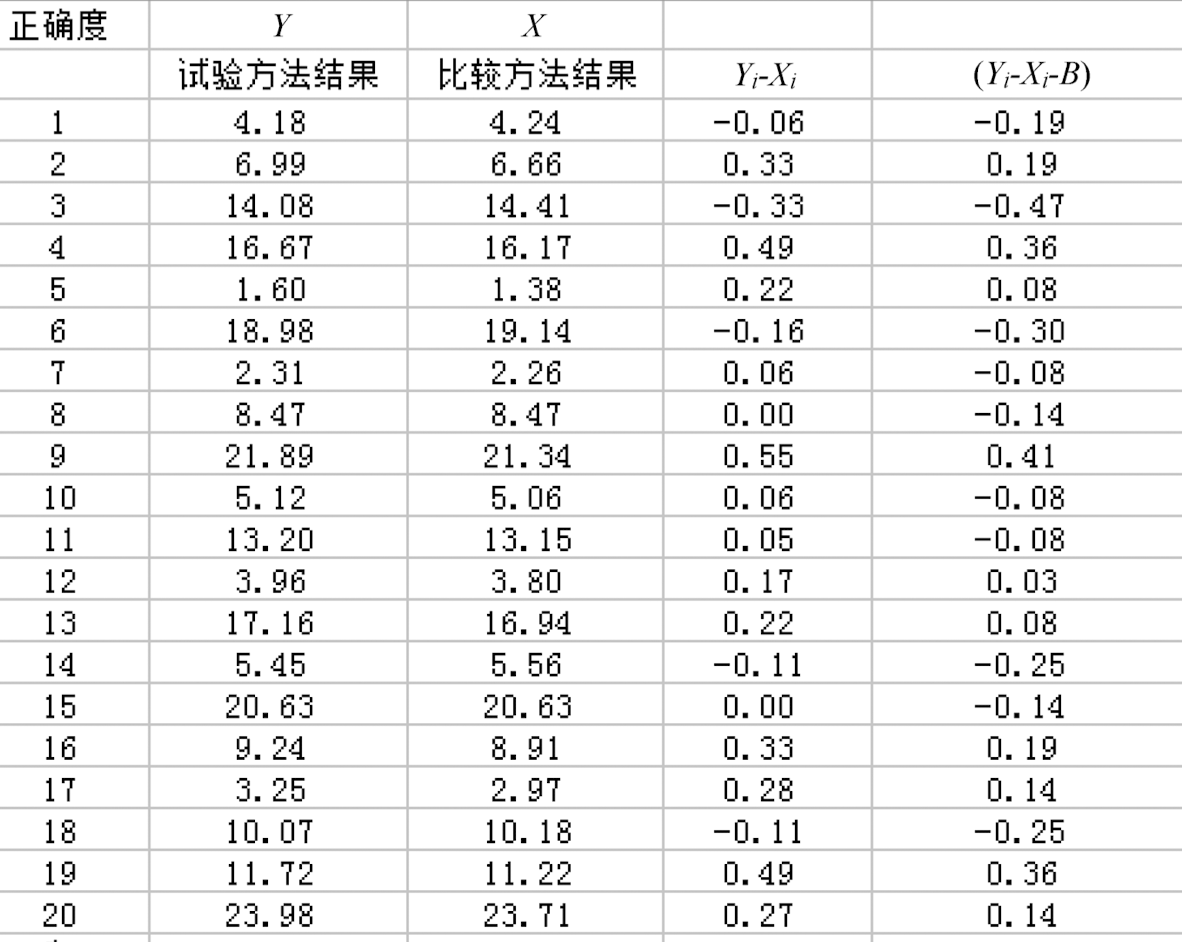
记录可以得到如下的数据稿
方法B:计算与验证
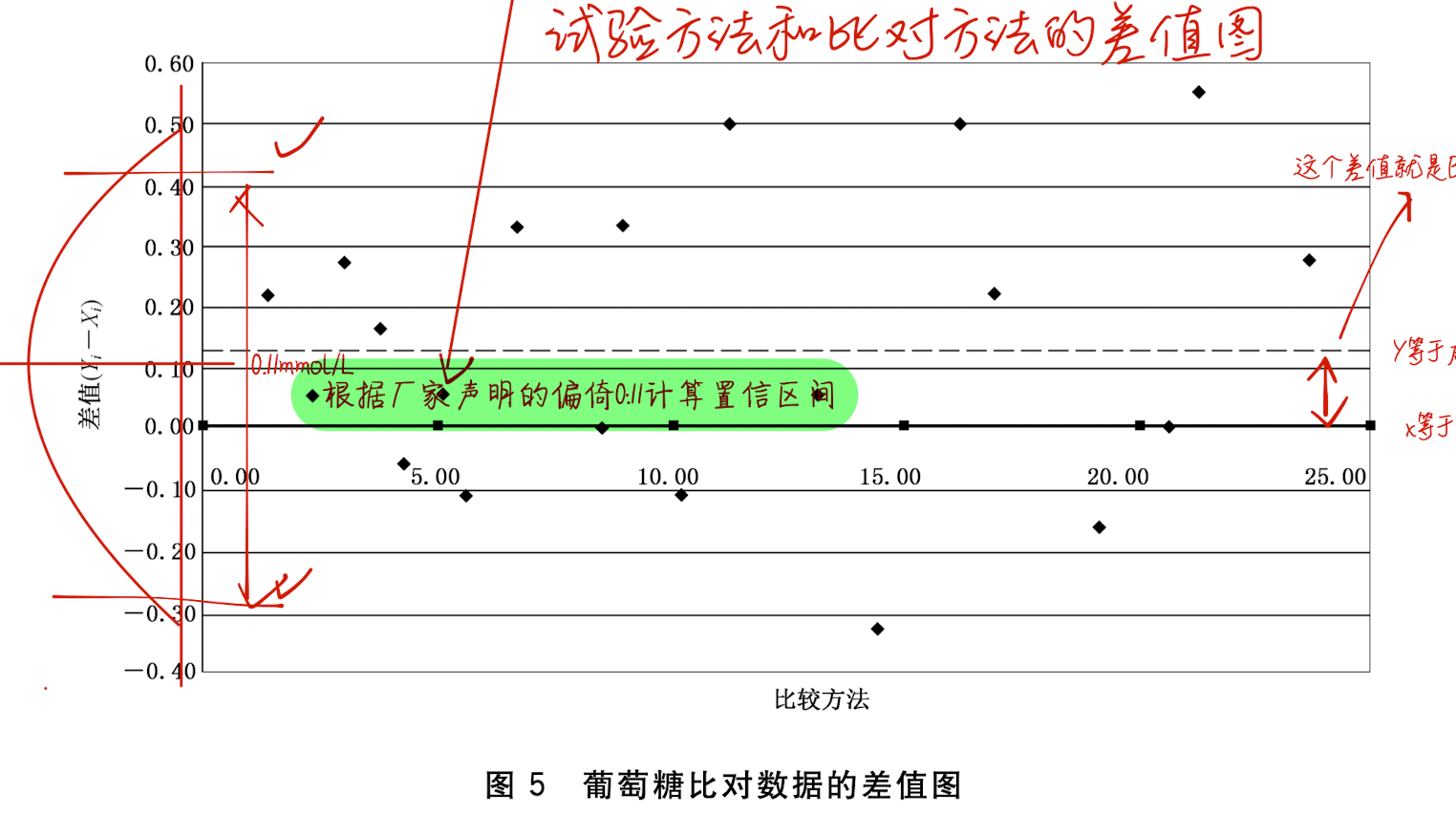
通过上面的数据,我们可以计算出Y的均值、X的均值、差值、差值标准差、再对厂家声明的偏倚计算出验证限。
如果实验室计算的偏倚,落在了验证限之内,即证明了厂家的声明。
当然这个过程如果用图形的方式表现出来,可能会更好。
以上就是对正确度验证的两种方法。
而这个方法B的最大的一个问题,就是一般情况下厂家是无法提供或声明项目偏倚的,解释起来又涉及到了生物变异、实验室质量管理的很多内容,如果大家感兴趣,我单独做一期视频跟大家讲一下。