临床可报告范围 CRR (Clinical reportable range)
关于这一部分,行标等文件并没有明确的描述,与至于,如何规定,如何做,到如何应用,也都是大家比较困惑的地方。
我之前也做过一个视频,关于线性和可报告范围的,那个时候,正好是我们科室经过了ISO15189的第二年,恰逢监督评审,于是我就此机会,也有幸认识了几位检验专家,对于这个困惑也向他们进行了咨询,不过遗憾的是,各位专家的意见是不一致的。
后来又有了一些其他同行的讨论,目前我比较中意的看法,如下图

这是新产业杨葆胜老师给我的参考课件。
如文中描述,在我们做线性的时候,并不能代表了其上下限,而是要通过功能灵敏度或者叫做定量检测线,和最大稀释倍数来确定最后的临床可报告范围(CRR)。很多朋友对这个可报告范围非常的困惑,其实就是因为说法太多了,所以再次做一些总结吧。
线性范围=可报告范围=分析测量范围=不经过稀释处理的。
临床可报告范围=经过稀释处理的报告范围,为什么要加上临床呢,因为有些项目临床上是有需求的,例如低值的Tsh、高值的Hcg,临床是需要更大的范围的,我们要做的就是通过线性验证、可报告范围验证来满足临床需求和检验本身的质量要求。
如何确定验证报告
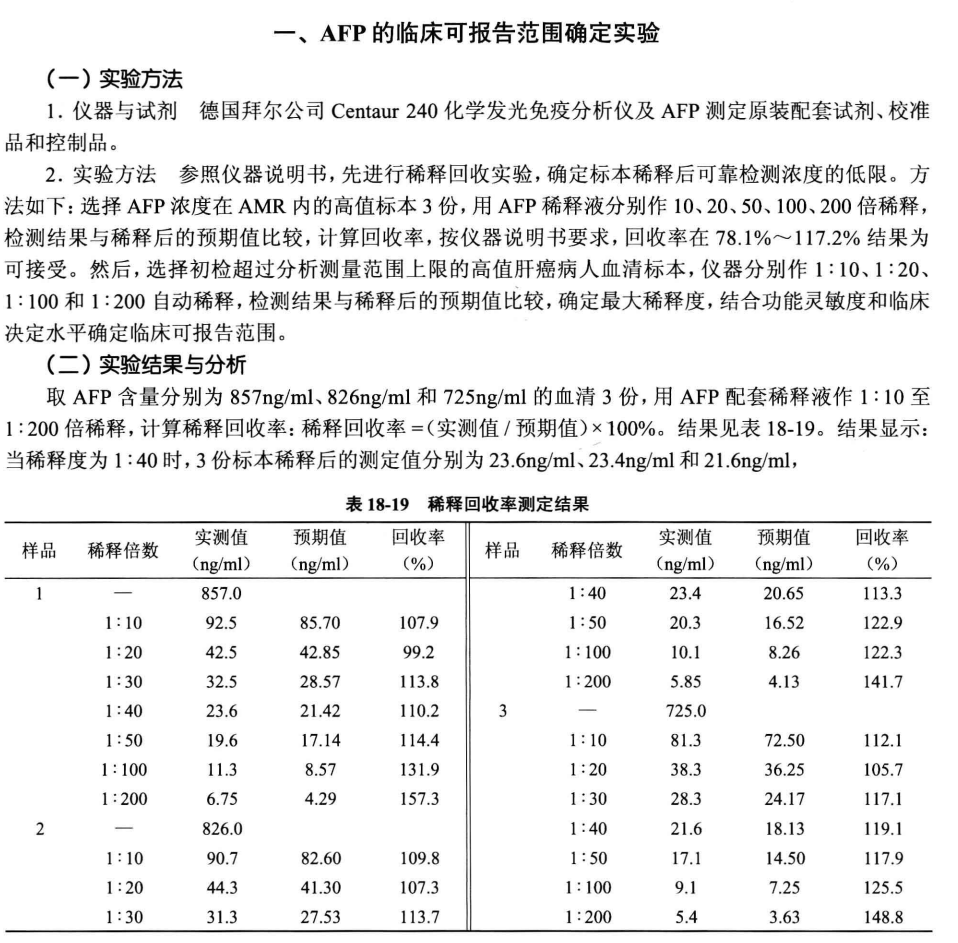
由于没有标准可遵循,所以我还是根据《临床生化检验诊断学》张秀明老师的这本书,其中有一个AFP的示例,拿来作为引用依据。
总体来说,通过这个可报告范围确定试验,我们可以得到4个结果。
1、标本稀释后可靠的检测浓度底限。也就是经过稀释的检测低值,这个值并不是LoQ,也就是说一旦您的标本经过了稀释操作,至少要大于该值,否者是不可靠的。
2、根据回收率的可接受范围,确定最大稀释倍数。
3、功能灵敏度或者定量检出限LoQ,这个是需要专门的验证程序的,对于低值有意义的时候,并不能简单的用AMR的线性低值作为该值,这样的的范围是不准确的
4、最大稀释度CRR的上限,AMR的上限*最大稀释倍数。
完整的报告内容,如下。